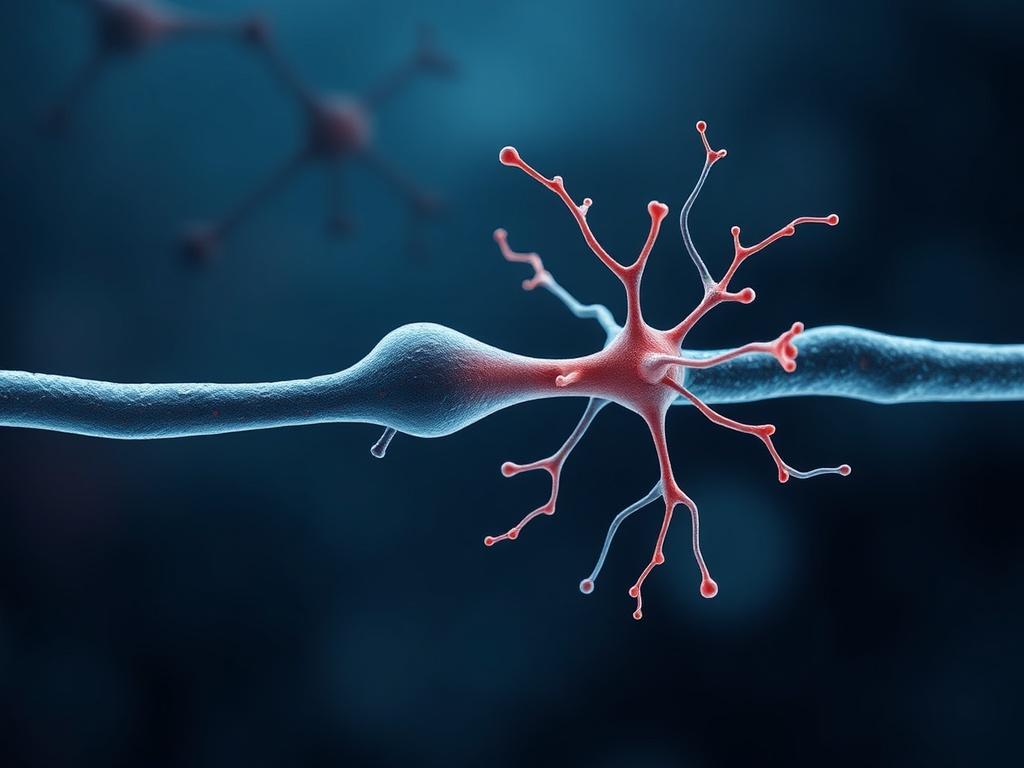
Когда я впервые увидел снимки нейронов под микроскопом, это был не просто набор линий и пятен, а целая вселенная с дорогами, перекрёстками и станциями. Строение нейрона и синапса — тема, которая на первый взгляд кажется сухой анатомией, но на деле раскрывает способы, которыми клетки превращают ионы и молекулы в ощущения, решения и воспоминания.
В этой статье я пошагово расскажу о ключевых компонентах нейрона, об электрофизиологии, о том, как передаётся сигнал через синапс, и почему все эти мелочи важны для работы мозга и медицины. Материал подан так, чтобы оставалось место для любопытства и для практических ассоциативных образов, а не только для формул и определений.
Нейрон: базовая единица нервной сети
Нейрон — это специализированная клетка, приспособленная для приёма, передачи и обработки информации. Его основная задача не просто проводить сигнал, а преобразовывать его, усиливать или подавлять в зависимости от входных импульсов и состояния сети.
Чтобы понять, как нейрон справляется с этими функциями, полезно рассмотреть его строение по частям: тело клетки, дендриты, аксон и специализированные структуры на концах. Эти элементы не случайны, каждый отвечает за определённый этап превращения входного стимула в выходной сигнал.
Сома — тело клетки
Сома, или перикарион, содержит ядро и большинство органелл: митохондрии, рибосомы, эндоплазматический ретикулум. Отсюда поддерживаются жизненные процессы клетки и синтезируются белки, необходимые для поддержания мембранных каналов и рецепторов.
В соме интегрируются входящие сигналы, поступающие по дендритам; именно здесь накапливается информация о сумме возбуждающих и тормозящих влияний. Если суммарный потенциал достигает порога, сома запускает ответ в виде потенциала действия, который дальше распространяется по аксону.
Дендриты — приёмные ветви
Дендриты — разветвлённые отростки, увеличивающие площадь приёма сигналов; их поверхность богата синапсами и рецепторами. Форма и ветвление дендритной системы сильно варьируются у разных типов нейронов, что отражает их функциональные роли: от тонкой настройки сенсорных сигналов до интеграции сложных ассоциативных потоков.
На дендритах часто встречаются шипики — небольшие выступы, где располагаются большинство возбуждающих синапсов. Эти структуры динамичны: при определённых условиях они могут изменять форму и число, что лежит в основе синаптической пластичности и обучения.
Аксон — линия передачи
Аксон — длинный, обычно тонкий отросток, по которому распространяется электрический сигнал, называемый потенциалом действия. Аксон может быть коротким или достигать десятков сантиметров в теле крупных животных, и он обеспечивает быструю передачу команд от перикариона к эффектору или другим нейронам.
На конце аксона находятся терминали, или синаптические окончания, где электрический импульс преобразуется в химический сигнал. Важную роль играют микротрубочки и аксональный транспорт — молекулы и органеллы доставляются вдоль аксона к синапсам и обратно.
Миелиновая оболочка и узлы Ранвье
У многих аксонов присутствует миелиновая оболочка — слой липидно-белкового вещества, изолирующий мембрану и ускоряющий проведение импульсов. Миелин вырабатывают специальные клетки: в периферии — шванновские клетки, в центральной нервной системе — олигодендроциты.
Между участками миелина остаются узлы Ранвье, где мембранные каналы сконцентрированы; проведение импульса происходит скачкообразно, от узла к узлу. Такое салтаторное проведение значительно повышает скорость и эффективность передачи информации в нервной системе.
Электрические основы работы нейрона
Работа нейрона опирается на электрохимию: разность потенциалов между внутренней и внешней средой клетки создаёт запас энергии для передачи сигналов. Это не магия, а точная балансировка ионных концентраций и селективной проницаемости мембраны.
Понимание мембранного потенциала и потенциала действия важно не только для биологии; эти принципы лежат в основе многих методов нейрофизиологии и терапии, включая стимуляцию и запись активности.
Потенциал покоя и ионные градиенты
Потенциал покоя обычно составляет около −60…−70 мВ и поддерживается работой натрий-калиевого насоса и ионных каналов. Натрий сконцетрирован вне клетки, калий — в еёнутри, и именно движение этих ионов через мембрану определяет электрический потенциал.
Нарушение этих градиентов ведёт к изменению возбудимости нейронов; поэтому электролитный баланс и энергетический резерв клетки критичны для нормальной работы. Клинически это проявляется в симптомах при отравлениях, гипокалиемии и других состояниях.
Потенциал действия: генерация и распространение
Если возмущение сома достигает порогового значения, открываются напряжённо-зависимые натриевые каналы, и внутрь клетки врывается поток Na+, вызывая фазу деполяризации. За ней следует открытие калиевых каналов и реполяризация: ионы K+ выходят наружу, восстанавливая мембранный потенциал.
Потенциал действия — это «всё или ничего»: его амплитуда не зависит от силы стимула, если порог достигнут. Скорость распространения определяется диаметром аксона и степенью миелинизации; большие миелинизированные аксоны проводят импульс быстрее.
Рефрактерность и кодирование информации
После активации нейрон входит в абсолютный и относительный рефрактерные периоды, когда новые потенциалы трудно или невозможно сгенерировать. Это ограничение задаёт максимальную частоту импульсов у данного нейрона и формирует базовые правила кодирования информации в виде частоты и временных паттернов.
Кодирование информации в нервной системе сочетает частотные и временные механизмы: частота импульсов передаёт интенсивность, а временная синхронизация между нейронами — вероятность связного восприятия событий. Именно поэтому изучение ритмов и синхронизации так важно для понимания функций мозга.
Синапс: место встречи нейронов
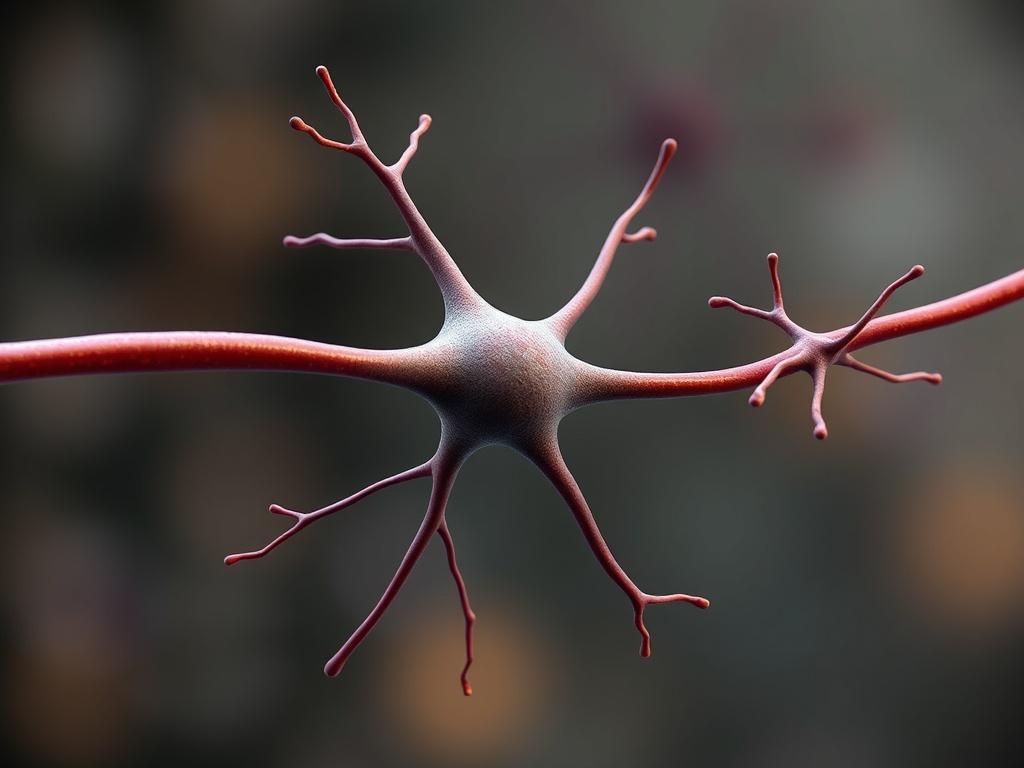
Синапс — это специализированный контакт между нейронами, где электрический сигнал одного клетки переходит в другой, чаще всего в химическом виде. Это место обмена информацией, где решается: усилить сигнал, подавить, задержать или изменить его качество.
Синапсы бывают разные по строению и механизму действия. Разбор их тонкостей помогает понять, как формируются поведенческие реакции и почему некоторые терапии работают полезно, а другие — вызывают побочные эффекты.
Химический синапс
В химическом синапсе пресинаптическая терминаль содержит пузырьки с нейромедиатором, который высвобождается в синаптическую щель по приходу потенциала действия. Нейромедиатор диффундирует к постсинаптической мембране и связывается с рецепторами, открывая ионные каналы или активируя внутриклеточные пути.
Химические синапсы позволяют гибко модулировать сигнал: различия в типах нейромедиаторов и рецепторов определяют, будет ли постсинаптическая клетка возбуждена или подавлена. Это обеспечивает богатство вычислительных возможностей нейронной сети.
Электрический синапс
Электрические синапсы устроены иначе: это щелевые контакты, или коннексины, которые создают прямые ионные мостики между клетками. Через такие соединения ток проходит быстро и без задержки, что важно для синхронной работы групп нейронов, например в сердечной ткани или некоторых рефлексивных цепях.
Электрические синапсы менее пластичны по сравнению с химическими, но они незаменимы там, где требуется молниеносная координация. В мозге они играют роль в синхронизации осцилляций и в поддержании ритмов, необходимых для работы сетей.
Пресинаптическая и постсинаптическая части
Пресинаптическая часть содержит молекулярный аппарат для упаковки, транспортировки и выделения нейромедиаторов: везикулы, белки синаптического слияния, насосы восстановления. Энергетическое обеспечение и кальциевый хоместаз в этой зоне особенно критичны для точного управления высвобождением.
Постсинаптическая мембрана богата рецепторами и молекулами сигналинга, которые определяют ответ клетки. Изменения количества и чувствительности рецепторов — один из способов, которым синапс регулирует свою силу в долгосрочной перспективе.
Молекулярный механизм передачи сигнала
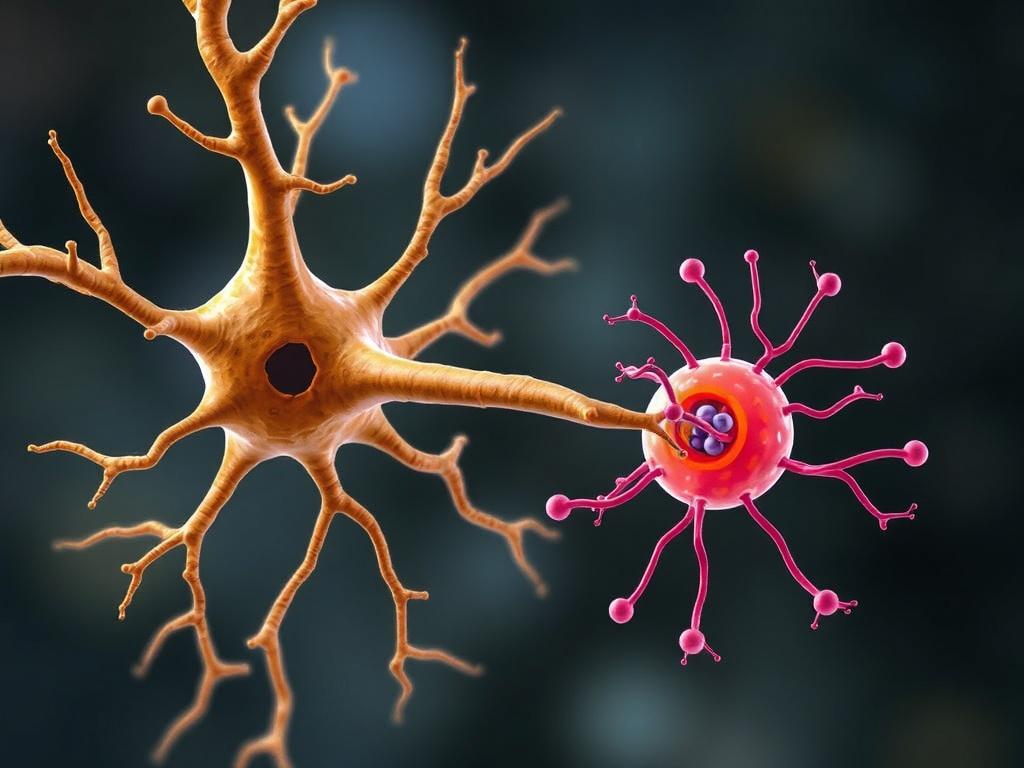
Молекулы, лежащие в основе синаптической передачи, разнообразны: классические нейромедиаторы, пептиды, газообразные посредники. Понимание их ролей помогает не только в биологии, но и при разработке лекарств, влияющих на настроение, боль и когнитивные функции.
Синтез, упаковка, высвобождение и уничтожение нейромедиаторов подчинены сложной координации белков и ионов. Малейшее нарушение в этих процессах может приводить к заметным изменениям в поведении или к патологии.
Нейромедиаторы и их судьба
Классические примеры нейромедиаторов — глутамат, ГАМК, ацетилхолин, дофамин, серотонин. Каждый имеет свои рецепторы и эффекты: глутамат обычно возбуждает, ГАМК — тормозит, а дофамин связан с мотивацией и вознаграждением.
После высвобождения нейромедиатор может быть удалён посредством обратного захвата пресинаптической мембраной, разложен ферментами или диффундировать из синапса. Механизмы утилизации важны для точности сигнала и предотвращения его длительного воздействия.
| Молекула | Основная роль | Пример влияния |
|---|---|---|
| Глутамат | Возбуждающий нейромедиатор | Учёт сенсорных сигналов, пластичность |
| ГАМК | Тормозящий нейромедиатор | Контроль возбудимости, анксиолитический эффект |
| Ацетилхолин | Передача в ПНС и CNS | Контроль мышечной активности, внимание |
| Дофамин | Модулятор мотивации и движений | Система вознаграждения, паркинсонизм при дефиците |
Синаптическая пластичность: основа обучения и памяти
Синаптическая пластичность — это способность синапсов изменять свою силу в ответ на активность. Эти изменения могут быть кратковременными и выражаться в изменении вероятности высвобождения нейромедиатора, либо долговременными, когда меняется число рецепторов или строение шипиков.
Два классических явления — долговременное потенцирование (LTP) и долговременное депрессионирование (LTD) — считаются молекулярным субстратом обучения. Они демонстрируют, как повторяемая активность может укреплять или ослаблять синапсы, формируя следы памяти в сети.
Механизмы LTP и LTD
LTP часто начинается с активации определённых рецепторов, например NMDA-рецепторов, и последующего притока кальция, что запускает каскады сигналинга и приводит к увеличению числа AMPA-рецепторов. Это повышает чувствительность постсинаптической мембраны к глутамату и усиливает синапс.
LTD может быть опосредовано меньшим поступлением кальция или активацией других путей, приводящих к удалению AMPA-рецепторов. В итоге сеть адаптируется: ненужные или шумные связи ослабляются, а важные — укрепляются, что обеспечивает гибкость и эффективность обработки информации.
Разнообразие нейронов и синапсов
Нейроны различаются по форме, по нейромедиаторному профилю, по функциональной роли и пластичности. В мозге человека встречаются миллиарды клеток самых разных типов, от простых сенсорных до сложных интернейронов, координирующих локальные и глобальные процессы.
Разновидности синапсов тоже впечатляют: кроме классических возбудительных и тормозных есть модуляторные синапсы, внешне имитирующие гормональный эффект, а также редкие электрические контакты. Это разнообразие обеспечивает богатую палитру вычислительных приёмов сетей.
- По морфологии: мультиполярные, биполярные, псевдоуниполярные нейроны.
- По функции: сенсорные, моторные, интернейроны, модуляторы.
- По нейромедиатору: глутаматергические, ГАМК-ергические, дофаминергические и т.д.
Методы изучения нейронов и синапсов
Современная нейронаука использует широкий набор инструментов — от классической гистологии до оптогенетики. Каждый метод даёт свой ракурс: кто-то показывает структуру, кто-то — электрическую активность, а кто-то — поведение клеток в живом организме.
Эти подходы часто комбинируют: микроскопия высокого разрешения позволяет увидеть шипики и везикулы, а электрофизиологические методы записать потенциалы действий и синаптические токи. Такое мультидисциплинарное изучение даёт полноценное понимание механики работы нейронов.
Классические и современные техники
Патч-кламп остаётся золотым стандартом для измерения тока через отдельные ионные каналы и для записи потенциалов действий. С помощью этой методики исследователи могут детально изучать свойства мембранных белков и механизм высвобождения нейромедиаторов.
Флуоресцентная микроскопия и суперрезолюционные методы позволяют визуализировать молекулярные комплексы в синапсе. Оптогенетика даёт возможность управлять активностью определённых классов нейронов с помощью света, что особенно ценно в экспериментах на живых животных.
Клиническое значение: когда строение даёт сбой
Нарушения структуры нейронов или синапсов лежат в основе множества заболеваний: рассеянный склероз — разрушение миелина, болезнь Альцгеймера — синаптическая потеря и накопление патологических белков, эпилепсия — нарушение баланса возбуждения и торможения.
Понимание молекулярных механизмов даёт путь к терапии. Лекарства, восполняющие дефицит нейромедиаторов или блокирующие патологические каналы, а также методы восстановления миелина, исследуются с целью вернуть утерянную функцию или приостановить прогрессирование болезни.
Примеры вмешательств
Антидепрессанты часто действуют за счёт модуляции обратного захвата серотонина или норадреналина, изменяя тонус системной модуляции. В случае Паркинсона используются препараты, повышающие дофаминовую передачу, а при эпилепсии — антиконвульсанты, уменьшающие чрезмерную возбудимость нейронов.
Кроме фармакологии, развиваются подходы генной и клеточной терапии, нейростимуляции и протезирования. Точные знания о строении и работе синапсов необходимы для создания эффективных и безопасных вмешательств.
Как эти знания применяются за пределами медицины
Идеи, почерпнутые из нейробиологии, вдохновляют разработчиков искусственного интеллекта: принципы пластичности и локальной обработки сигналов используются при создании нейронных сетей и алгоритмов обучения. Здесь заимствованы не биологические детали, а общие принципы организации и адаптации.
Кроме того, понимание нейрональной коммуникации важно для создания нейроинтерфейсов и протезов, которые должны «говорить» на том же языке, что и нервная система. Это сочетание инженерии, биологии и этики, где точность в деталях имеет решающее значение.
Личный опыт: почему меня захватило это ремесло
В юности я писал заметки о микрофотографиях, словно описывал пейзажи неизведанных миров. Позже я работал в лаборатории, где под моим микроскопом впервые подсветили синапсы флуоресцентной меткой — это ощущение открытия трудно передать словами, оно больше похоже на встречу с хорошо знакомым другом, который вдруг показывает неожиданные черты характера.
Эти практические наблюдения, возможно, объясняют мой подход к объяснению сложного: стремление не просто перечислять факты, а связывать их с образами и ситуациями, которые помогают запомнить и применить знания. Я видел, как одна малюсенькая молекула может изменить поведение нейронной сети и, как следствие, биологического организма.
Практические советы для тех, кто хочет углубиться
Если вы только начинаете изучать нейробиологию, начните с базовой электрофизиологии и морфологии: эти две линии знания помогут вам связать функцию с формой. Чтение статей и просмотр учебных видеолекций будет полезным, но пытайтесь регулярно смотреть реальные данные — графики, микрофотографии, записи активности.
Работа с экспериментальными данными учит думать по-нейронному: оценивать шум, искать закономерности и учитывать биологическую вариативность. Не бойтесь простых вопросов — часто именно они приводят к важным открытиям.
Последние мысли и приглашение к размышлению
Строение нейрона и синапса раскрывает, как из мельчайших деталей складывается поведение целого организма и индивидуальный опыт. Понимание этих элементов не только удовлетворяет научное любопытство, но и даёт практические инструменты для медицины, инженерии и образования.
Если вы хотите продолжить знакомство с темой, начните с конкретного вопроса: например, как изменяется синаптическая сила при хроническом стрессе, или какие молекулы ответственны за долгосрочную память. Маленькие шаги в изучении нейрона и синапса постепенно складываются в богатую картину работы нервной системы.